Hvert år får cirka 20-30 barn i Norge et nytt organ, enten et nytt hjerte, lever eller nyre. Siden oppstarten av solid organtransplantasjon av barn i Norge på slutten av 1960-tallet er over 600 barn transplantert. Det økende antall pasienter som blir transplantert bidrar til økt behov for kunnskap utenfor transplantasjonsmiljøet. Hva bør du som barnelege vite om immundempende legemidler?
Tekst: Kari Christiane Fougner Bjerknes, klinisk farmasøyt ved Avdeling for barnemedisin og transplantasjon. Anna Bjerre, overlege/ professor og fagansvarlig pediatrisk nefrologi. Thomas Möller, overlege/ forsker, fagansvarlig hjerte-Tx, Barnekardiologisk avdeling. Anniken Bjørnstad Østensen, overlege og fagansvarlig lever. Samtlige forfattere: Barne- og ungdomsklinikken, Oslo universitetssykehus. Foto: Øystein Horgmo, UiO
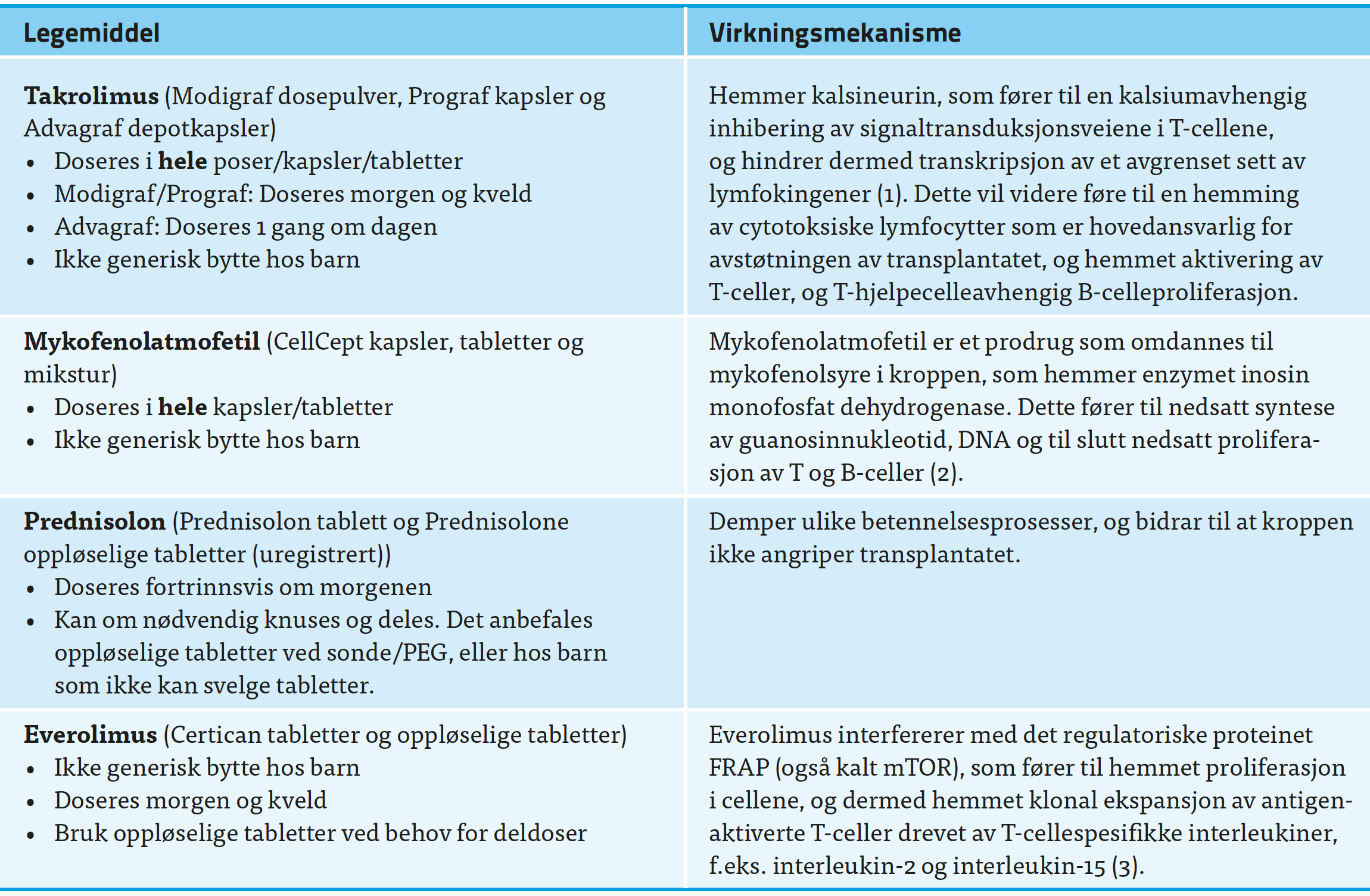
Ved transplantasjon er det behov for livslang immundempende behandling for å unngå organavstøtning. Ved solid organtransplantasjon er gullstandarden å starte behandlingen med takrolimus, mykofenolatmofetil og prednisolon, og i tiden rett etter transplantasjon er det nødvendig med høye doser på grunn av et aktivt immunforsvar. Avhengig av organ og pasient kan prednisolon vurderes seponert etter 4-6 måneder. Det brukes forskjellig intensitet i immunsuppresjon avhengig av type organ som blir transplantert: høyere doser og legemiddelkonsentrasjoner for hjerte og lunger enn for nyre og lever. Benmargstransplantasjon vil ikke bli diskutert i denne teksten.
Balanse og justeringer
Det er en fin balanse mellom tilstrekkelig immunsuppressiv behandling og færrest mulig bivirkninger, og å samtidig unngå organavstøtning og langtidskomplikasjoner. For lite immunsuppresjon øker risikoen for avstøtning. For mye immunsuppresjon øker infeksjonsfare og kreftrisiko. For takrolimus, og til en viss grad mykofenolatmofetil, er det derfor ønskelig å skreddersy dosen til pasienten. Dette gjøres ved å måle bunnkonsentrasjon av takrolimus, som tas rett før ny dose skal gis (på folkemunne kalt speil). Dosen justeres etter ønsket konsentrasjon i henhold til transplantasjonsprotokollene. Det tas hyppige konsentrasjonsmålinger i starten, med avtagende frekvens det første året. Deretter kontrolleres takrolimus ved faste kontroller og eventuelt på indikasjon, som ved sykdom. Mykofenolatmofetil kontrolleres vanligvis ved oppstart, eventuelt med jevnlige AUC-målinger (areal under kurven for plasmakonsentrasjon mot tid), og ved mistanke om over- eller underdosering.
For barn anbefales det at takrolimus og mykofenolatmofetil tas til samme tidspunkt hver dag, med 30 minutters faste av både mat og andre legemidler før og etter inntak. Absorpsjonsgraden av takrolimus øker ved faste, og det er ønskelig med færrest mulige faktorer som kan påvirke opptaket av legemidlene. For pasienter hvor fasting ikke er gjennomførbart er det viktig å tilstrebe at det gjøres likt hver gang, slik at mat eller legemidler kan utelukkes hvis det er store variasjoner i fullblodskonsentrasjon.
Sykdom
Ved sykdom er det nødvendig å kontrollere takrolimus ekstra, da konsentrasjonen kan bli sterkt påvirket og risikoen for toksiske doser er større. Spesielt gjelder dette ved oppkast eller diaré. Et tett samarbeid mellom lokalsykehuset og Rikshospitalet er nødvendig. Mekanismen bak økt konsentrasjon ved diaré skyldes endret opptak av takrolimus i tarmen. Normalt vil absorpsjonen av legemidlet bli regulert av PGP-pumper i tarmslimhinnen, som pumper takrolimus tilbake i tarmen og minsker systemisk opptak. Ved diaré blir disse pumpene trolig satt ut av spill, og mindre legemiddel blir pumpet tilbake igjen i tarmen. Dermed øker absorpsjonen av takrolimus, som potensielt kan gi økte bivirkninger og toksiske doser.
Nedsatt immunforsvar
Behandling med takrolimus og mykofenolatmofetil demper immunforsvarets aktivitet, og særlig det spesifikke immunsystemet. Dermed svekkes kroppens immunrespons mot bakterier, virus, sopp og kreftceller. Pasientene er derfor mer mottakelig for infeksjoner og virusreaktiveringer. Selv «ufarlige » og opportunistiske infeksjoner som ikke-transplanterte barn vanligvis klarer å bekjempe, kan bli en utfordring. Dette gjelder blant annet vannkopper. For transplanterte barn som ikke har hatt vannkopper, kan sykdommen bli livstruende. Forebyggende behandling med aciklovir eller valaciklovir (Zovirax / Valtrex) skal gis ved mistanke om eksponering. Anbefalinger rundt dette finnes i Veileder i generell pediatri, kap. 3.22.
De første 6 månedene bruker pasientene trimetoprim/ sulfametoksasol (Bactrim) forebyggende mot Pneumocystis jirovecii-pneumoni. For pasienter som har mottatt et CMV-positivt organ, og ikke selv har gjennomgått CMV-infeksjon, brukes valganciklovir (Valcyte) forebyggende i 3-6 måneder. Siden immunforsvaret er dempet hos transplanterte barn, skal de aldri ha vaksiner med levende virus. Inaktiverte vaksiner kan gis. Nyinfeksjon eller reaktivering av Epstein-Barr-virus etter en transplantasjon kan få alvorlige forløp som ved PTLD (post-transplant lymphoproliferative disease). Livstidsrisikoen for sekundær kreftsykdom økes ved livslang immunsuppresjon.

Ved organtransplantasjon er medisineringen skreddersydd hver enkelt pasient.
Bivirkninger og komplikasjoner
De fleste legemidler gir bivirkninger, og de immundempende legemidlene er intet unntak. Bivirkningene opptrer gjerne ved oppstart av behandlingen og er forbigående, men noen kan også oppstå etter langtidsbruk. Kvalme og diaré er vanlige bivirkninger av mykofenolatmofetil, og i noen tilfeller reduseres dosen hvis bivirkningene er for plagsomme. Mykofenolatmofetil er teratogent, og ungdom som bruker legemidlet skal bruke prevensjon. Legemidlet skal seponeres hos begge kjønn i god tid før planlagt graviditet, i samarbeid med oppfølgende instans. For både mykofenolatmofetil og takrolimus anbefales moderat soleksponering, og bruk av solkrem ved sterk sol. Dette skyldes at huden lett kan bli solbrent, samt at risikoen for hudkreft øker ved langtidsbruk. Uønskede effekter av takrolimus kan være høyt blodtrykk, og det er ikke uvanlig at barna bruker blodtrykksenkende legemidler i en periode etter transplantasjon. Man bør og kjenne til at 60-70% av barna som bruker takrolimus utvikler hypomagnesemi, og de kan også oppleve hodepine, skjelvinger, søvnproblemer, håravfall og synsendringer. Nyrefunksjonen påvirkes også av takrolimus, spesielt ved høye doser, og i noen tilfeller kan det medføre behov for å redusere dosen eller endre immunsuppresjonen.
Everolimus (Certican) er en mTor-hemmer som er mindre nyretoksisk. Denne brukes ofte sammen med takrolimus, eventuelt i forløpet av PTLD. Bytte av immundempende behandling skal alltid skje i samråd med lege tilhørende Avdeling for barnemedisin og transplantasjon eller Barnekardiologisk avdeling ved OUS.
Noen barn får høyt blodsukker etter transplantasjonen, og kan utvikle diabetes. Prednisolon gis i høye doser etter transplantasjon, og det er ikke uvanlig å oppleve bivirkninger som økt appetitt og økt vekt, høyt blodtrykk, søvnløshet og humørsvingninger. Bivirkningene avtar som regel når dosen reduseres.
Tilleggsbehandling og interaksjoner
Transplanterte barn bruker ofte en kombinasjon av legemidler. Som et fotballag kreves det flere spillere for å komme i mål. Vitamintilskudd og blodtrykkssenkende legemidler er ofte nødvendig. Alle bruker forebyggende trimetoprim/sulfametoksasol i en periode etter transplantasjon, samt eventuelt valganciklovir. Enkelte har behov for blodfortynnende og protonpumpehemmer, og hjertetransplanterte barn bruker i tillegg statiner livet ut. Behandlingen er skreddersydd den enkelte pasient.
Ved oppstart av nye legemidler bør det alltid sjekkes for interaksjoner. Takrolimus metaboliseres via CYP3A4 og CYP3A5 i leveren, og samtidig bruk av legemidler som påvirker CYP-enzymene kan gi endring av takrolimuskonsentrasjonen i blodet. Eksempler på slike legemidler er flukonazol og erytromycin, og ved bruk av disse bør det gjennomføres konsentrasjonsmålinger av takrolimus for å vurdere dosejustering. Det er viktig å være klar over at også visse typer mat kan interferere med takrolimus, slik at bunnkonsentrasjonen endres. CYP3A4/CYP3A5 har en genetisk betinget variabilitet som krever forskjellige doser takrolimus for å oppnå et visst konsentrasjonsområde. Forekomsten av genetiske varianter henger sammen med etnisitet.
Samarbeid
En vellykket behandling av transplanterte barn avhenger av tett oppfølging, og samarbeid på tvers av fag og nivåer. God kommunikasjon mellom pasient, lokalsykehus, apotek og transplantasjonsavdelingen er avgjørende. Fagmiljøet på Rikshospitalet bistår gjerne ved spørsmål! Prosedyrer fra Barne- og ungdomsklinikken finnes i økende omfang i internettversjonen av OUS eHåndbok (https:// ehandboken.ous-hf.no/). På sikt vil mange prosedyrer og anbefalinger rundt organtransplantasjon hos barn bli tilgjengelig der.
Kilder: 1.
- Preparatomtale Prograf: https://www.legemiddelsok.no/_layouts/15/ Preparatomtaler/Spc/1997-03113.pdf
- Preparatomtale Cellcept: https://www.ema.europa.eu/en/documents/ product-information/cellcept-epar-product-information_no.pdf
- Preparatomtale Certican: https://www.legemiddelsok.no/_layouts/15/ Preparatomtaler/Spc/03-2079.pdf
- Informasjonsskriv om de ulike preparatene fra Nasjonalt kompetansenettverk for legemidler til barn: https://www.legemidlertilbarn.no/ barnogforeldre/Sider/Nettverkets-legemiddelinfo.aspx